 左図は、水の電気分解の概略を表したものである。
左図は、水の電気分解の概略を表したものである。
「水素水」は明確に定義された用語ではありません。
ここ数年何かと話題になっている「水素水」の話。
その効能の程や、抑々「水素水」とやらの実在性すら怪しいところであるが、本稿ではその「水素水」について述べる。
「水素水」として市販されている商品には、以下のようなものがあるようだ。[注1]
水素原子は単独の形(水素ラジカル H·)では安定して存在できるものではない。
商品によっては H6O や H14O といった分子の形で多くの水素原子を含んでいるとするものもあるが、こういった分子も存在し得ない。
(分子とは原子同士が電子を共有することで成立するものであるが、H6O や H14O では共有できる電子が足りない筈である。)
従って、原子としての水素原子が豊富に含まれるとする商品は、全くの偽りであると言える。
水素イオン H+ も同じく、それ自体は安定して存在できるものではない。
「水素イオン」という用語自体は高校化学等では頻出であるが、実際には水分子 H2O と結合してオキソニウムイオン H3O+ の形で存在するものである。
仮に「オキソニウムイオンが豊富」という意味なのだとしたら、それはただの酸性の液体である。
そうなると、「水素水」として存在し得るのは、水素分子 H2 が豊富に含まれるものぐらいということになる。
効能はさておき、確かに水素は水に溶けるので、「水素分子が豊富に含まれる」水素水というのは存在し得る。
(尤も水素が水に溶ける量は微々たるものである)
では、どうやって水素を水に溶かしているのだろうか?
水素を水に溶かすには、十分な量の水素を水と一緒に封入し、圧力を高くする。
この水素は、水を電気分解することで作ることができる。[注1]
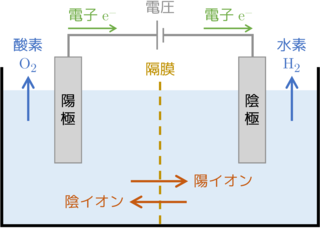
 左図は、水の電気分解の概略を表したものである。
左図は、水の電気分解の概略を表したものである。
水を隔膜で2つに隔てたそれぞれに電極を入れて電圧を印加する。
すると、陰極側で水素が、陽極側で酸素が発生する。
これが水の電気分解である。
(電極や水中の電解質に依っては異なる反応が生じるが、本稿では省略する)
この陰極側の水を水素と共に封じ込めたものが、所謂「水素水」である。[注1]
水の電気分解によって、陰極側では以下の現象が起こる。
こうして得られた金属イオンを含むアルカリ性の水は、まさに所謂アルカリイオン水或いは電解還元水に他ならない。[注2]
結論: 「水素水」の正体は、「アルカリイオン水」だった。
^ a b c 1. 筆者は「水素水」として市販されているものの全貌を把握している訳ではないので、本稿で考慮している範疇の外のものが存在する可能性は勿論ある。
^ 2. 「アルカリイオン水」の「アルカリ」の指すところは「アルカリ金属/アルカリ土類金属のイオン」とも「アルカリ性」とも取れるが、いずれにせよこれはアルカリイオン水と呼ばれるものである。(当ページでは以前は前者の説を採っていたが、「アルカリ性電解水」という言葉との整合性を考えると後者と捉える方が妥当とも考えられる)